Это все очень вдохновляет, но нужно объяснить и последний кусочек головоломки: почему только два электрона могут занимать каждый энергетический уровень? Так утверждает принцип Паули, и он очень важен для связи в единое целое всего, что мы обсуждаем. Без него электроны толпились бы на низшем энергетическом уровне вокруг каждого ядра, и никакой химии не было бы. Это не самая приятная перспектива, потому что тогда не было бы молекул, а следовательно, и жизни на Земле.
Утверждение о том, что каждый энергетический уровень могут занимать два и только два электрона, кажется каким-то произвольным. До того как эта идея была впервые предложена, никто не высказывал предположений по этому поводу. Первый прорыв в этой области был совершен Эдмундом Стоунером, сыном профессионального игрока в крикет (который прошел восемь калиток в игре с Южной Африкой в 1907 году, если вы читаете Wisden Cricketers’ Almanack) и бывшим студентом Резерфорда, впоследствии возглавившим физический факультет в Университете Лидса. В октябре 1924 года Стоунер предположил, что на каждом энергетическом уровне (n, l, m) должно находиться два электрона. Паули развил идеи Стоунера и в 1925 году опубликовал правило, которому годом позже Дирак присвоил его имя. Принцип Паули состоит в том, что ни одна пара электронов в атоме не может иметь одни и те же квантовые числа. Однако он столкнулся с проблемой: все указывало на то, что на самом деле два электрона могут иметь одинаковый набор значений n, l и m. Паули обошел проблему, просто введя новое квантовое число. Это был анзац: он не знал, чему соответствует это число, но оно могло принимать одно из всего двух значений. Паули признавался: «Более точно причин существования этого правила мы указать не можем». Новое открытие случилось в 1925 году и было изложено в работе Джорджа Уленбека и Сэмюэла Гаудсмита. В поисках возможности проведения точных измерений атомных спектров они связали дополнительное квантовое число Паули с реальным физическим свойством электрона, которое носит название спин
[32].
Основная идея спина довольно проста и восходит еще к 1903 году: она значительно старше квантовой теории. Через несколько лет после открытия собственно электрона немецкий физик Макс Абрахам предположил, что электрон – это мельчайшая вращающаяся электрически заряженная сфера. Если бы это было верно, то электроны подвергались бы действию магнитных полей в зависимости от ориентации поля по отношению к оси их вращения. В статье 1925 года, опубликованной через три года после смерти Абрахама, Уленбек и Гаудсмит отмечали, что модель вращающегося шара не может быть верной, потому что для подтверждения экспериментальных данных электрон должен вращаться быстрее скорости света. Но сам дух идеи был верен: у электрона действительно есть свойство под названием спин, которое действительно влияет на его поведение в магнитном поле. Однако на самом деле идея спина – это непосредственное и довольно тонкое последствие теории специальной относительности Эйнштейна, получившее должную оценку только после того, как Поль Дирак в 1928 году записал уравнение, описывающее квантовое поведение электрона. Для наших целей сейчас нужно только указать, что существует два типа электрона, которые мы будем называть «спин вверх» и «спин вниз». Они отличаются противоположными значениями момента вращения, то есть словно бы вращаются в противоположных направлениях. Очень жаль, что Абрахам лишь немного не дожил до открытия истинной природы спина электрона, потому что так и не отказался от своего подозрения, что электрон – это мельчайшая сфера. В некрологе Абрахаму в 1923 году Макс Борн и Макс фон Лауэ писали: «Он был достойным оппонентом, сражался достойным оружием и не старался замаскировать поражения причитаниями и не относящимися к делу аргументами… Он любил свой абсолютный эфир, свои уравнения поля, свой неподвижный электрон, как повзрослевший человек любит свою первую страсть, воспоминания о которой не затмит никакой последующий опыт». Если бы все наши оппоненты были такими, как Абрахам!
В оставшейся части этой главы мы попытаемся объяснить, почему электроны ведут себя столь странным образом, описанным в принципе Паули. Как обычно, постараемся по максимуму использовать наши квантовые циферблаты. Для этого подумаем, что произойдет при «отталкивании» электронов друг от друга. На рис. 7.3 показан конкретный сценарий, когда два электрона, помеченные цифрами 1 и 2, начинают свое движение в одном месте и заканчивают в каком-то другом. Конечные точки мы отметили буквами А и В. Заштрихованные круги напоминают, что мы пока не думали по поводу того, что случается при взаимодействии двух электронов друг с другом (подробности этого процесса для нынешних целей не имеют особого значения).
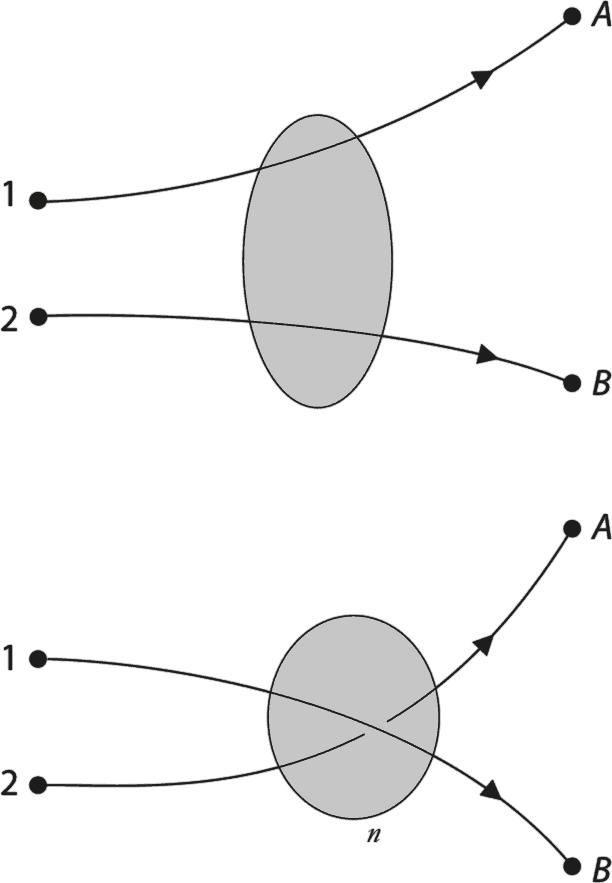
Рис. 7.3. Разлет двух электронов
Нужно представить, что электрон 1 выпрыгивает из исходной точки и заканчивает движение в точке А. Точно так же электрон 2 «приземляется» в точке В. Это показано на верхней иллюстрации. На самом деле аргумент, который мы намерены предъявить, прекрасно работает, даже если игнорировать возможность взаимодействия электронов. В этом случае электрон 1 попадает в точку А независимо от любых блужданий электрона 2, и вероятность найти электрон 1 в точке А и электрон 2 в точке В будет всего лишь произведением двух независимых вероятностей.
Например, представим, что вероятность прибытия электрона 1 в точку А равна 45 %, а вероятность электрона 2 в точку В – 20 %. Вероятность нахождения электрона 1 в точке А и электрона 2 в точке В равна 0,45 × 0,2 = 0,09 = 9 %. Здесь мы пользуемся обычной логикой, которая говорит, что вероятность подбросить монетку, чтобы выпал орел, и вместе с тем бросить кубик, чтобы выпала шестерка, равны ½ × ⅙, что составляет 1/12 (то есть чуть больше 8 %)
[33]. Как показано на иллюстрации, у электронов есть и другой способ оказаться в точках А и В. Электрон 1 может попасть в точку В, а электрон 2 – в точку А. Допустим, вероятность найти электрон 1 в точке В равна 5 %, а вероятность найти электрон 2 в точке А – 20 %. Тогда вероятность найти электрон 1 в точке В и электрон 2 в точке А равна 0,05 × 0,2 = 0,01 = 1 %.
Таким образом, у нас есть два варианта нахождения двух электронов в точках А и В – один с вероятностью 9 % и один с вероятностью 1 %. Таким образом, вероятность того, что один электрон будет в точке А, а другой в точке В, если не имеет значения, какой где окажется, должна составлять 9 % + 1 % = 10 %. Все просто; но неверно.



