Установлено, что активная циркуляция эндогенных основных желчных кислот (дезоксихолевой и хенохолевой) вызывает физиологическую блокаду ядерных FXR-рецепторов в гепатоците, аналогично той, что наступает в постпрандиальном периоде и маркирует поступление в печень большого количества алиментарных жиров. Этот базовый эндокринный механизм активирует основной обмен, липолиз и окисление ЖК, препятствует накоплению в печени ТГ, уменьшает инсулинорезистентность [61].
Однако важнейшей целью нутрицевтической коррекции является коррекция жирового рациона, не только как его наиболее калорийной части, но и как прямого стимулятора эктопического отложения жира и причины провоспалительной деформации внутренней среды организма. Согласно международному консенсусу, доля «жирных калорий» в рационе для лечения НАЖБП не должна превышать 30–35 % от суммарной калорийности, а доля калорий, полученных из насыщенных жиров, должна быть менее 7 % от общей калорийности рациона. Поступление холестерина с пищей не должно превыщать 200 mg/dL при обязательном исключении употребления транс-жиров. Основным источником жирных калорий должны быть 8-10 г/сутки жиров с полиненасыщенными жирными кислотами (ПНЖК) [53–56].
В качестве модели для построения лечебного пищевого рациона при НАЖБП международный консенсус клинических практических рекомендаций предлагает Средиземно-морскую диету (уровень доказательности В1) [47,51]. Средиземноморская диета как понятие была введена в медицинскую практику после 1960 года, когда Ансель и Маргарет Кейс опубликовали результаты эпидемиологического исследования «Seven Countries’ Study», согласно которым в 7 странах средиземноморского бассейна заболеваемость ССЗ и раком оказалась значительно ниже, чем в США, Северной Европе и Японии [62].
Отличительными признаками Средиземно-морской диеты являются:
✓ высокое потребление свежих фруктов, овощей, картофеля, бобов, орехов, кунжута, льняного семени и других семян;
✓ хлеб, макаронные изделия и другие продукты на основе зерновых культур:
✓ оливковое масло для готовки и заправок, а также и другие источники жиров, которые не содержат насыщенные жирные кислоты, обеспечивающие 25–35 % суммарной калорийности;
✓ умеренное потребление кисломолочных продуктов из цельного молока и йогуртов;
✓ умеренное употребление рыбы и морепродуктов, изредка — мясо;
✓ умеренное потребление красного вина, обычно во время приема пищи;
✓ выбор свежих сезонных продуктов [63].
Начиная с 70-х годов, во множестве теоретических и экспериментальных исследований было показано, что Средиземноморская диета является оптимальным рационом для сохранения здоровья, снижения риска ССЗ и ожирения, хронических дегенеративных заболеваний, уменьшения массы тела [64, 65, 66]. В новейших исследованиях на фоне Средиземноморской диеты уменьшалась жировая инфильтрация печени и лабораторные проявления НАСГ (уменьшение AST/ALT) [67–69]. В ряде работ, по данным авторов, приверженность Средиземноморской диете приводила к увеличению чувствительности к инсулину у больных с инсулинорезистентностью даже без достижения существенного уменьшения массы тела [70–72].
Эффективность Средиземноморской диеты и близких к ней рационов питания («северный рацион»: рыба + капуста + ржаной хлеб + овсяная каша + яблоки + корнеплоды или «восточный рацион»: рыба + морепродукты + продукты из сои и других бобовых + столовая зелень) обусловлена высоким содержанием в ней пищевых источников антиоксидантов и незаменимых (эссенциальных) для человека ПНЖК [73].
В указанных продуктах со-3 ПНЖК могут содержаться в свободной форме (α-линоленовая кислота в семенах, орехах, водорослях, растительных маслах — кроме оливкового; эйкозапентаеновая и докозагексаеновая кислоты в жирной морской рыбе) или в форме эссенциальных фосфолипидов (бобовые, соя, яичный желток, цельное молоко). Для поддержания «здоровья» клеточных мембран организма и успешной борьбы с оксидативным стрессом пищевой рацион современного горожанина должен содержать не менее 2 г взаимозаменяемых ω-3 α-линоленовой/эйкозапентаеновой и 6–8 г со-6 линолевой/арахидоновой ПНЖК из любых пищевых источников или из биологически активных добавок и лекарственных препаратов [74]. Доказано, что при перманентном поступлении с пищей ПНЖК насыщают фосфолипиды клеточных мембран, чем и обусловлено их кардиопротективное, антиаггрегантное и противовоспалительное действие как системное в печени (табл. 5) [75–77].
Таблица 5
Этнические различия в содержании мембранных фосфолипидов в тромбоцитах (модифицировано по Rodriguez-Leyva D. et al. 2009) [76]
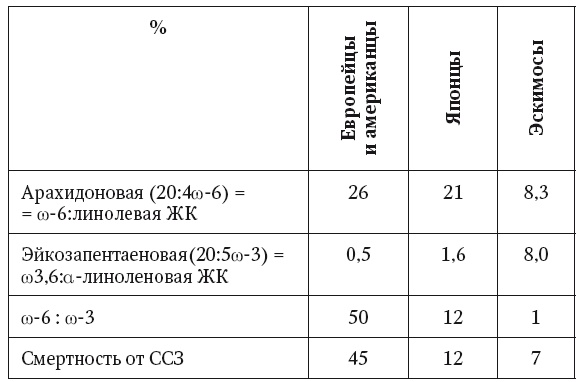
Однако важнейший механизм лечебного действия ПНЖК, особенно со-3 α-линоленовой и эйкозапентаеновой жирных кислот, при НАЖБП обусловлен их антиатерогенным влиянием на липидный обмен: способностью активировать окисление ТГ и уменьшать жировую инфильтрацию печени, минимизировать последствия липотоксичности и уменьшать инсулинорезистентность во всех тканях-мишенях, а также препятствовать избыточному синтезу холестерина и его обратному всасыванию в кишечнике (табл. 6) [22, 23, 78, 79].
Таблица 6
Интегральное влияние ω-3ПНЖК на липидный обмен и его нарушения при НАЖБП [22, 23, 78].

Больным с морбидным ожирением (ИМТ > 30 кг/м2) рекомендованы все стратегии снижения веса, за исключением назначения адрено-позитивных препаратов (сибутрамин). С осторожностью должны назначаться препараты, вызывающие диарею и нарушающие энтерогепатическую циркуляцию желчных кислот (орлистат), стимулирующие жировую инфильтрацию печени. У пациентов с НАСГ сегодня активно рассматривается безопасность бариатрической хирургии. Очевидно, что схемы с выведением из пищеварения повздошной кишки, как и длительная терапия орлистатом, пациентам с НАСГ противопоказаны.
Согласно международным клиническим рекомендациям, медикаментозная терапия показана только пациентам с верифицированным НАСГ и значимым уровнем фиброза печени (> F2), пациентам с СД, метаболическим синдромом и стойким повышением АЛТ (уровень доказательности В1). Такой осторожный подход рекомендован для терапии инсулиносенситайзерами: пиоглитазоном (высокая частота побочных эффектов — увеличение веса, остеопороз, сердечная недостаточность) и высокими дозами витамина Е (увеличивают риск канцерогенеза и тромботических осложнений), при том что оба метода лечения приводят к улучшению гистологической структуры у пациентов с НАСГ (уровень доказательности В1). Несмотря на потенциальное гепатотоксическое действие, пиоглитазон рекомендован для применения у больных НАСГ, однако с оговорками, что убедительных данных о безопасности при длительном приеме нет и его можно назначать только после гистологической верификации НАСГ. Близкую позицию эксперты Американской ассоциации по изучению заболеваний печени занимают по витамину Е. Показано, что у больных с НАСГ длительная терапия витамином Е в дозе 800 мг/ сутки оказывает выраженное антиоксидантное действие и приводит как к гистологическому, так и к клинико-лабораторному улучшению. В рекомендациях 2016 года было вновь почеркнуто, что терапия метформином (А1) и УДХК (В1) не оказывает значимого влияния на гистологию печени при НАЖБП и не рекомендована как метод специфической терапии НАСГ у взрослых. Доказано, что метформин, который широко применяется для уменьшения инсулинорезистенотности, приводит к снижению массы тела, ингибированию глюконеогенеза и липогенеза в печени, стимуляции β-окисления жирных кислот и улучшению клинико-лабораторного профиля пациентов. Однако в целом ряде исследований терапия метформином при НАСГ не сопровождалась гистологическим улучшением. Это привело к коррекции его места в клинических рекомендациях, но совершенно не отменяет необходимости назначения метформина как препарата 1 выбора для лечения инсулинорезистентности при MC и СД 2 типа.




