Это открытие привело к некоторому пересмотру представлений в данной области. Если стресс продолжается достаточно долго и начинает подавлять иммунитет, некоторые элементы, традиционно считавшиеся свидетельством подавления иммунитета, на самом деле оказались признаками его укрепления.
Это проявляется двумя способами. Если кто-то принимает большую дозу глюкокортикоидов или в течение многих часов подвергается действию очень мощного стрессора, то его гормоны начнут уничтожать лимфоциты без разбора, просто убивать их. Если ненамного повысить уровень глюкокортикоидов (так происходит в начале фазы В), то гормоны будут уничтожать только определенную подгруппу более старых лимфоцитов, которые и так неэффективны. На этом этапе глюкокортикоиды помогают укреплять иммунную реакцию, избавляясь от лимфоцитов, бесполезных в текущей чрезвычайной ситуации. Это является косвенным подтверждением укрепления иммунной функции.
Вторая тонкость отражает новую интерпретацию того, что люди знали испокон веков (по крайней мере во времена Селье). Как мы уже знаем, глюкокортикоиды не только уничтожают лимфоциты, но и вытесняют из крови еще оставшиеся в ней лимфоциты. Фирдаус Дабар из Университета штата Огайо решил выяснить, куда деваются иммуноциты, которые вытеснены из крови. Всегда считалось, что все они оправляются в хранилища в иммунных тканях (например, в тимус). Они дезактивируются, и от них уже нет никакой пользы. Но работа Дабара показывает, что не все они отправляются на консервацию. Глюкокортикоиды и адреналин отправляют многие из этих лимфоцитов к месту инфекции, например в кожу. То есть иммуноциты не дезактивируются, а отправляются на передовую. Поэтому, например, царапины на коже заживают быстрее.
Таким образом, в начале действия стрессора глюкокортикоиды и другие гормоны, реагирующие на стресс, ненадолго активируют иммунную систему, улучшая иммунную защиту, оттачивая ее, доставляя иммунные клетки к месту битвы с инфекцией. Но если действие глюкокортикоидов продолжается, система может промахнуться и войти в аутоиммунное состояние. Поэтому при длительном стрессе возникает обратный эффект: система возвращается к базовой линии. Во время патологического сценария, когда на организм действуют сильные и длительные стрессоры, иммунитет падает ниже базовой линии.
Эти новые открытия помогают объяснить один из самых упрямых парадоксов в этой области. Он касается аутоиммунных заболеваний.
Вот два факта об аутоиммунных процессах:
1. Поскольку аутоиммунные заболевания связаны с избыточной активацией иммунной системы (до такой степени, что здоровые функции и органы тела она начинает воспринимать как агрессора), самое распространенное и освященное веками лечение таких болезней состояло в том, чтобы посадить пациента «на стероиды», давая ему большие дозы глюкокортикоидов. Логика здесь очевидна: это резко подавляет иммунную систему и она больше не может нападать на поджелудочную железу, нервную систему или на какой-то другой объект своего неуместного рвения (и, как очевидный побочный эффект этого подхода, иммунная система также будет не слишком эффективно защищать пациента от реальных патогенов). Поэтому назначение больших доз гормонов стресса облегчает симптомы аутоиммунных болезней. Кроме того, выяснилось, что длительное действие сильных стрессоров снижает симптомы аутоиммунных заболеваний у лабораторных крыс.
2. В то же время, по-видимому, стресс может усугублять аутоиммунные заболевания. Стресс—один из самых надежных факторов (если не самый надежный), ухудшающих прогноз при таких заболеваниях. Об этом часто сообщают пациенты, и не менее часто это игнорируют врачи, которые знают, что гормоны стресса облегчают аутоиммунные состояния, а не ухудшают их. Но некоторые объективные исследования также подтверждают эту гипотезу, например для таких аутоиммунных заболеваний, как рассеянный склероз, ревматоидный артрит, диффузный токсический зоб, язвенный колит, воспалительные заболевания кишечника и бронхиальная астма. Сейчас есть всего несколько таких отчетов, и многие им не доверяют, потому что они основаны на ретроспективных данных, взятых из самоотчетов пациентов, а не на научных экспериментах. Однако результаты довольно однородны: у многих больных дебют аутоиммунных заболеваний, и в еще большей степени их периодические обострения, коррелирует со стрессом. Кроме того, к настоящему времени уже есть довольно обширная литература, подтверждающая, что стресс может ухудшать симптомы аутоиммунных заболеваний у животных.
Так как же действуют глюкокортикоиды и стресс — они ухудшают или облегчают симптомы аутоиммунных заболеваний? Приведенный ниже график дает ответ, который не удавалось найти раньше. Мы обнаружили два сценария, которые увеличивают риск аутоиммунных заболеваний. Во- первых, кажется, что многочисленные кратковременные стрессоры (то есть многократное прохождение фаз А и В) увеличивают риск аутоиммунных процессов. Почему-то повторяющиеся подъемы и спады ведут систему вверх, повышая вероятность аутоиммунных заболеваний. Во-вторых, не очень полезно, когда много раз за фазой А идет фаза В, но если за фазой А не возникает фаза В, это также увеличивает риск аутоиммунного процесса. Если нет адекватной фазы В, начинает раскручиваться спираль иммунной системы и возникает аутоиммунный процесс (рис. 30).
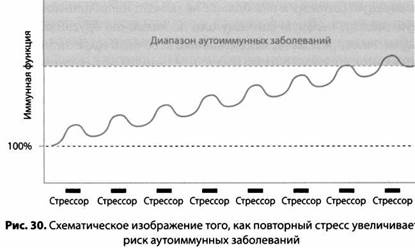
Как и следовало ожидать, если вместо этого мы имеем сильные и длительные стрессоры или вводим в организм большие дозы глюкокортикоидов, то система перейдет в фазу С — возникнет мощное подавление иммунной функции, уменьшающее аутоиммунные симптомы. Эту гипотезу поддерживает еще одно открытие: острый стресс увеличивает у крыс риск рассеянного склероза, а хронический стресс подавляет симптомы этого аутоиммунного заболевания. Очевидно, в процессе эволюции система не была предназначена для того, чтобы иметь дело с многочисленными повторными «включениями/выключениями», и поэтому возникает нарушение координации, увеличивая риск аутоиммунных процессов в системе.
Хронический стресс и риск заболеваний
В этой книге мы уже много раз говорили о том, что определенная физиологическая реакция на обычные для млекопитающих стрессоры — если она длится слишком долго или возникает слишком часто — приводит к серьезным проблемам. Способность сильных стрессоров подавлять иммунитет ниже базовой линии — одна из таких проблем. Насколько опасно стрессогенное подавление иммунитета, если оно уже возникло? Как научил нас вирус СПИДа, если иммунная система серьезно подавлена, то 30-летний человек будет медленно умирать от рака и пневмонии, которые раньше врачи, за 50 лет своей карьеры, наблюдали только у пожилых пациентов. Но может ли хронический стресс подавлять иммунную систему до такой степени, чтобы вызывать болезни, которые иначе не возникли бы? А если мы уже заболели, то насколько труднее нам будет выздороветь?
Данные из множества источников свидетельствуют о том, что стресс действительно способен ослаблять иммунную систему и увеличивать риск заболеваний. Но, несмотря на это поразительное открытие, остается совершенно неясным, в какой степени хронический стресс делает нас уязвимыми к болезням, которые иммунная система обычно уничтожает в зародыше. Чтобы не запутаться в хаосе, который царит в этой сфере исследований, попробуем разложить их результаты на составные части.



