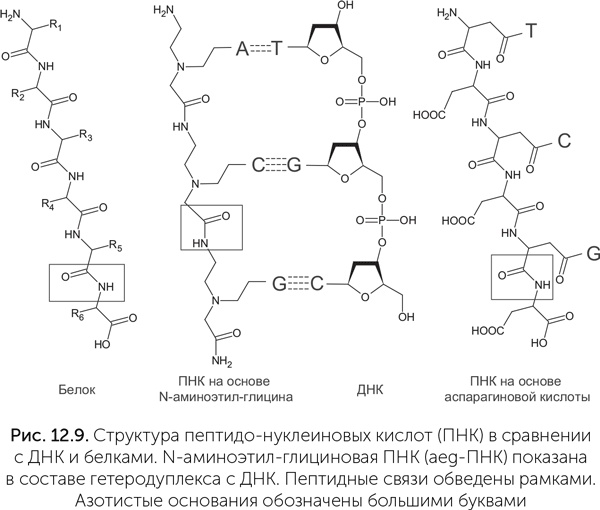
Пептидо-нуклеиновые кислоты
Кроме ТНК и ГНК были предложены и более радикальные альтернативы РНК, такие как пептидо-нуклеиновые кислоты (ПНК) (Nelson et al., 2000). Эти молекулы состоят из пептидной цепочки, сходной с таковой в белках, к которой присоединены азотистые основания (рис. 12.9). Пептидная цепь может состоять из разных аминокислот, не обязательно входящих в стандартный набор 20 белковых аминокислот. Пептидный остов отличается большей стабильностью по сравнению с любыми вариантами сахарофосфатного остова. Наиболее изучен вариант ПНК, остов которого состоит из звеньев N-аминоэтил-глицина (aeg-ПНК). Такая ПНК образует двойную спираль сама с собой и устойчивые гетеродуплексы с ДНК и РНК. В отличие от природных нуклеиновых кислот и большинства ксенонуклеиновых, звенья aeg-ПНК не содержат хиральных центров и не могут иметь левых и правых изомеров. Спираль, однако, имеет левую и правую формы. Одиночная нить aeg-ПНК может принимать и право-, и левоспиральную форму в гетеродуплексах с правой (природной) и левой ДНК. Двухцепочечная aeg-ПНК может легко менять хиральность спирали в зависимости от того, какие хиральные молекулы прикрепляются к ее концам. Значит, жизнь на основе aeg-ПНК могла отложить решение проблемы хиральной чистоты на более поздние этапы.
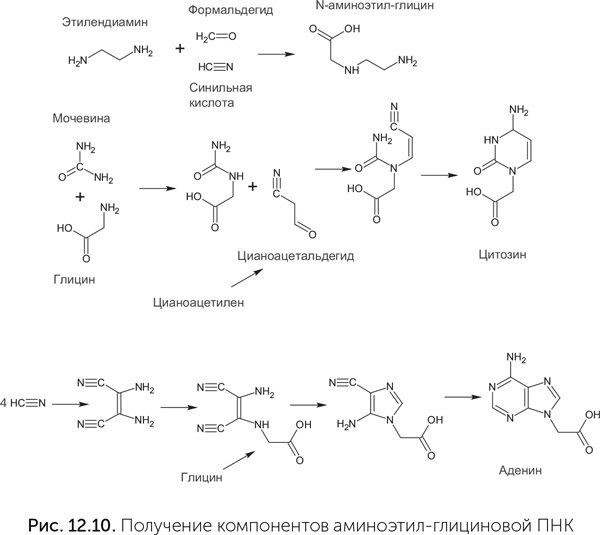
Для компонентов aeg-ПНК известен достаточно надежный абиогенный путь синтеза (Nielsen et al., 2007). Облучение растворов синильной кислоты с добавлением глицина и формальдегида дает одновременно N-аминоэтил-глицин для остова и четыре азотистых основания с ацетатными боковыми группами, которые нужны для их соединения с пептидным остовом (рис. 12.10).
Простой абиогенный синтез и отсутствие хиральности делают aeg-ПНК привлекательной в качестве главной молекулы древнейшей жизни, но другие ее свойства могут этому препятствовать. Как мы уже обсуждали, для хранения генетической информации лучше подходят молекулы с распределенным по всей длине электрическим зарядом, который мешает им свернуться в клубки. С одной стороны, aeg-ПНК не заряжена, и длинные ее цепи должны быть склонны к компактному сворачиванию. К сожалению, во время экспериментов пока исследовались только короткие, менее 20 звеньев, цепи ПНК. С другой стороны, в качестве катализатора ПНК благодаря компактному сворачиванию может быть лучше, чем РНК.
Более подходящий для хранения генетической информации вариант ПНК имеет остов из остатков аспарагиновой или глутаминовой кислоты, соединенных пептидными связями, как в обычных белках. Азотистые основания здесь прикрепляются к боковым COOH-группам аминокислот через одну. Половина СООН-групп остается свободной и обеспечивает отрицательный электрический заряд по всей длине молекулы (Mittapalli et al., 2007). К сожалению, пути абиогенного синтеза такой ПНК неизвестны. Так что пока мы не можем указать ни один конкретный полимер, который мог быть предшественником РНК, и никаких следов таких полимеров в биохимии не сохранилось.
Жизнь без полимеров
Еще более радикальной альтернативой РНК-мира стали гипотезы протометаболических циклов. Согласно им на древней Земле сначала сложилась сеть химических реакций между малыми молекулами, аналогичная реакциям обмена веществ в клетках. Катализаторами этих реакций служили минералы и сами участвующие в них малые молекулы. Нуклеотиды появились как один из продуктов этой сети реакций. Возникновение РНК, рибозимов, а затем и белков лишь придало устойчивость и увеличило скорость этой сети реакций.
Конечно, теория РНК-мира не отрицает, что какие-то реакции между малыми молекулами стали источником нуклеотидов и предшествовали появлению РНК. Разногласия между гипотезой протометаболических циклов и гипотезой РНК мира (в широком смысле, включая ПНК и другие полимеры, способные к комплементарному соединению в двойные спирали; в англоязычной литературе эти группы гипотез называются metabolism-first и replication-first) заключаются в другом. В гипотезе протометаболических циклов предполагается, что сеть реакций была способна к эволюции и усложнению, т. е. у нее могло быть много вариантов, каждый из которых был способен воспроизводить себя. Такое наследование, где сохраняется и воспроизводится химический состав смеси реагирующих веществ, получило название композиционного, или концентрационного генома. Теория РНК-мира же предполагает, что наследование, а следовательно, и дарвиновская эволюция возможны только на основе полимерных молекул.
В большинстве версий протометаболической гипотезы в качестве исходной части сети реакций обмена веществ рассматривается центральный круговорот обмена веществ – цикл Кребса. В статье Лесли Оргела (Orgel, 2008) рассматриваются препятствия для прохождения этого цикла реакций на минералах без помощи ферментов. Серьезной проблемой становится специфичность катализа. Например, в восстановительном цикле Кребса двойная связь C=C в одном случае должна восстанавливаться (при образовании янтарной кислоты), а в другом – к ней должна присоединяться молекула воды (при превращении аконитовой кислоты в лимонную). Если аконитовая кислота подвергнется восстановлению (а в тех условиях, где идет восстановительный цикл Кребса, эта реакция будет необратима), то вещество будет уходить из цикла в побочную реакцию. Аналогично, если какой-то минерал катализирует распад лимонной кислоты на уксусную и щавелевоуксусную, то он же будет вызывать распад и других кислот цикла.
Есть и другие мнения о том, какие вещества составляли первые автокаталитические циклы. Например, Альберт Эшенмозер предполагает (Eschenmoser, 2007), что исходным веществом, питающим цикл, был не углекислый газ, а синильная кислота (HCN). Молекулы синильной кислоты в воде самопроизвольно объединяются по четыре, образуя тетрамер. Эти тетрамеры при нагревании или облучении превращаются в аденин и гуанин, а при низкой температуре и в темноте постепенно подвергаются гидролизу. При этом образуются органические кислоты, близкие к кислотам цикла Кребса, – гидрокси-щавелевоуксусная, дигидрокси-фумаровая. Дальше из этих кислот могут получаться простейшие сахара (гликольальдегид, глицеральдегид) и более сложные кислоты цикла Кребса, такие как лимонная. Важно, что альдегиды (формальдегид, ацетальдегид, гликольальдегид) ускоряют сборку тетрамеров синильной кислоты и образуются в ходе гидролиза этих же тетрамеров. Иными словами, здесь возможно образование разных автокаталитических циклов и накопление многих веществ, важных и в современной биохимии.
К сожалению, в ходе экспериментов так и не удалось провести эти реакции достаточно эффективно, чтобы заработал автокатализ и производительность цикла стала расти. Для восстановительного цикла Кребса, как мы упоминали в прошлой главе, удалось провести только шесть реакций из одиннадцати. В качестве источника энергии при этом использовалось ультрафиолетовое излучение, а катализатором служили кристаллы сульфида цинка (Guzman, Martin, 2009).

