Однако ситуация не столь проста, как видно из результатов долгосрочных экспериментов с эволюционирующими популяциями кишечной палочки, проведенных Ричардом Ленски и его коллегами. Эти эксперименты показывают, что интенсивный отбор на адаптацию бактериальных популяций к новой среде часто ведет к появлению аллелей-мутаторов (иными словами, бактерий с повышенной частотой мутаций в связи с повреждением одного из ферментов репарации), которые вытесняют предыдущие поколения с низкими показателями мутаций (Sniegowski et al., 1997). Если быть более точным, представляется, что аллели-мутаторы достигают значительного распространения в популяции и даже фиксируются за счет тесного сцепления с адаптивными мутациями, вызываемыми этими мутаторами. Однако, когда внешнее селективное давление убрано, мутаторы становятся невыгодными и вымываются отбором (Denamur and Matic, 2006). Эти результаты приводят к важному обобщению: в зависимости от целого ряда факторов, таких как экологический стресс и эффективный размер популяции, отбор на низкую или высокую частоту мутаций может происходить и происходит в действительности.
Частота ошибок транскрипции гораздо выше, нежели частота ошибок репликации, а ошибки трансляции случаются еще более часто (см. рис. 9-4). Хотя экспериментальные измерения уровня ошибок включения аминокислот в ходе трансляции немногочисленны и ограничены несколькими модельными системами, все же ясно, что точность трансляции удивительно низка. В самом деле, частота встраивания ошибочных аминокислот составляет 10–4—10–5 — любопытно, что она близка к частоте ошибок репликации у РНК-вирусов. Получается, что около 20 процентов белковых молекул, синтезируемых в любой из клеток, содержат по меньшей мере одну неверную аминокислоту (Drummond and Wilke, 2009). Последствия ошибок транскрипции и трансляции, иногда метко называемых фенотипическими мутациями, очевидно, менее критичны, чем последствия генетических мутаций, по той причине, что фенотипические мутации, как правило, не наследуются (существуют примечательные исключения, например обратная транскрипция с последующим включением в геном ДНК-копии ошибочно транскрибируемой РНК; Burger et al., 2006). Учитывая сравнительно короткий срок жизни любой РНК или белковой молекулы, никакая фенотипическая мутация сама по себе не может оказать серьезного влияния на выживаемость, поэтому неудивительно, что для фенотипических мутаций допустимы гораздо более высокие частоты ошибок, чем для генетических мутаций. Однако столь же очевидно, что чрезмерно высокие темпы фенотипических мутаций несовместимы с жизнью. А значит, как и в случае с системами репарации ДНК, многочисленные механизмы, служащие для отслеживания ошибок транскрипции и трансляции, безусловно, существуют. Было показано, что коррекционная активность ДНК-зависимой РНК-полимеразы уменьшает процент ошибок на несколько порядков (Alic et al., 2007; Sydow and Cramer, 2009). Кроме того, также были открыты остающиеся пока слабоизученными процессы посттранскрипционного исправления ошибок метилирования в РНК (Begley and Samson, 2003; Falnes, 2005). Вероятно, из механизмов, контролирующих частоту фенотипических мутаций, лучше всего исследована коррекция аминоацил-тРНК-син тетазой (АРСазой), при которой молекулы аминоацил-тРНК, связанные с ошибочными аминокислотами, гидролизуются и утилизируются (Hussain et al., 2010; Ling et al., 2007). Упомянутая коррекция АРСазой дополняется рибосомной коррекцией на следующей стадии трансляции, при которой рибосома отбраковывает ошибочно связанные тРНК (Blanchard et al., 2004; Daviter et al., 2006). Однако значительное увеличение надежности трансляции, по-видимому, вступает в противоречие с требованием высокой скорости синтеза белка. Существенное повышение точности трансляции может быть легко достигнуто путем мутации конкретных позиций в рРНК или в рибосомных белках, но эти мутации оказываются вредными для клеток, по-видимому, из-за медленной трансляции (Dong and Kurland, 1995; Johansson et al., 2008).
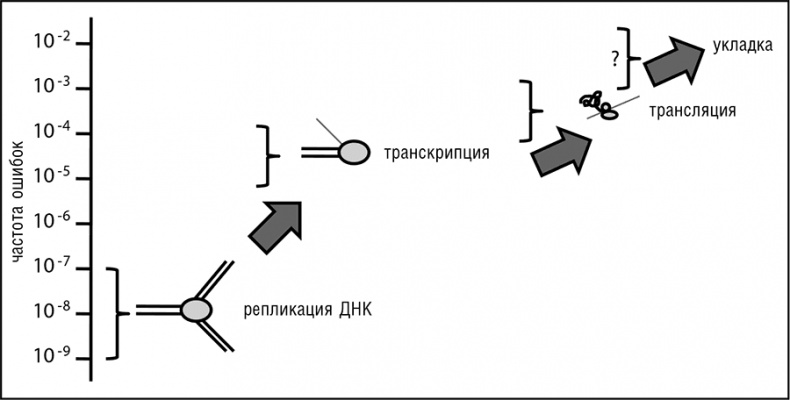
Рис. 9-4. Типичные частоты ошибок на различных стадиях передачи биологической информации.
Эксперименты с точными, но медленными рибосомными мутантами позволяют предположить, что компромисс между скоростью и точностью трансляции связан с механическими ограничениями трансляционной системы и с трудом может быть преодолен мутациями в ее компонентах. В результате для ограничения ошибок трансляции и их пагубных последствий эволюция, похоже, выбрала другие способы адаптаций.
Твердо установлено, что «высокостатусные» гены (те, что интенсивно экспрессируются и медленно эволюционируют) обладают более выраженным предпочтением триплетов по сравнению с «низкостатусными» генами. Оптимальные триплеты, которыми насыщены гены с высоким статусом, обеспечивают более низкую частоту ошибок, равно как и более высокую скорость трансляции, и, таким образом, частично избегают вышеупомянутого компромисса (Drummond and Wilke, 2009, 2008). Асимметрия триплетов между высокостатусными и низкостатусными генами может объясняться ценой селекции; в силу этого заметный отбор оптимальных кодонов может идти только в генах высокого статуса.
Основным вредным эффектом ошибок трансляции считается неправильная укладка белка (Drummond and Wilke, 2009, 2008), хотя ошибки включения аминокислот в каталитических сайтах, безусловно, могут стать дополнительным фактором. Как уже говорилось в главе 4, отбор на устойчивость к неправильной укладке является одним из главных аспектов эволюции белков — возможно, даже ее основной движущей силой. Менее ясно, какой источник неверной укладки наиболее важен — изначально неправильная последовательность или ошибки при ее трансляции. В любом случае, хотя укладка белка обычно не рассматривается в качестве процесса передачи информации, в действительности она им является. В самом деле, укладка предполагает поток информации, идущий от одномерной аминокислотной последовательности к трехмерной структуре белка.
Ровно то же самое относится к структурным РНК. Частоту неправильной укладки трудно определить экспериментально, и этого не было сделано для большого числа белков или РНК. Если тенденция, отражающая процент ошибок и показанная на рис. 9-4, — чем дальше от генома, тем менее точен этап передачи информации, — служит каким-либо индикатором, частота ошибок укладки должна быть даже выше частоты ошибок трансляции.
Такое предсказание также следует из здравого смысла, учитывая невероятную сложность процесса укладки и огромное количество ошибочных вариантов, доступных в принципе для укладываемого белка или РНК-молекулы (Bowman et al., 2011; Pande et al., 1998). Имея в виду высокую сложность пространства укладок, эпохальное открытие (сделанное первоначально Кристианом Анфинсеном и впоследствии подтвержденное многочисленными экспериментами), что белки способны самопроизвольно складываться в нативную конформацию, вызвало огромное удивление (Anfinsen, 1973).
Спустя почти 50 лет после открытия Анфинсена все еще остается предметом споров, глобальный или локальный минимум свободной энергии ищут спонтанно укладывающиеся белки. Но стало ясно, что лишь небольшие белки укладываются спонтанно; большинство белков нуждаются в специальных молекулярных устройствах, других белках, известных как шапероны, чтобы сформировать правильную структуру. Шапероны функционируют удивительным образом: их молекулы образуют «ячейку» (известную также как ячейка Анфинсена), которая изолирует укладываемый белок от цитоплазмы и частично разворачивает его, облегчая тем самым поиск нативной конформации (Ellis, 2003). Большинство шаперонов — синтезируемые в больших количествах, высококонсервативные, высокостатусные белки.



