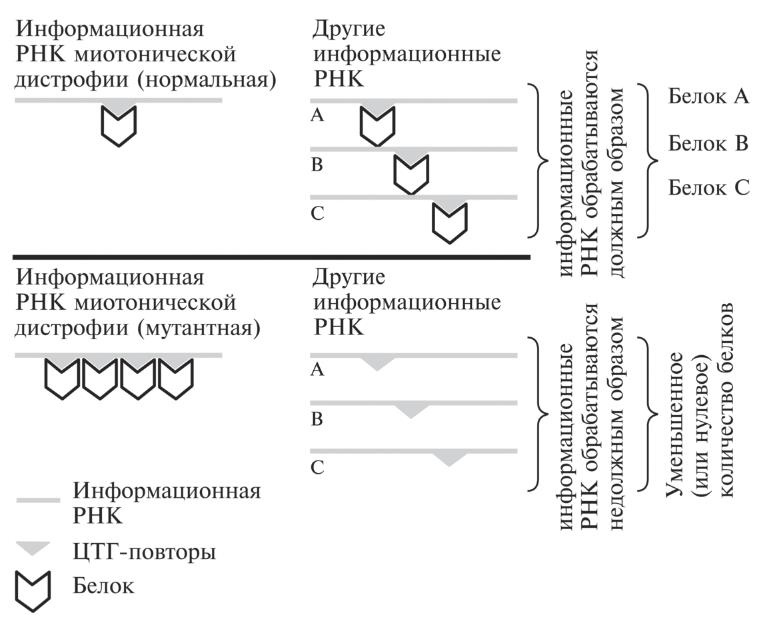
Рис. 16.4. Избыточное связывание белков с увеличенным при миотонической дистрофии количеством повторов определенного триплета в информационной РНК приводит к тому, что белки отбираются от других молекул информационной РНК, которые эти белки должны регулировать (происходит так называемая секвестрация белков). Другие информационные РНК перестают обрабатываться должным образом, что нарушает процесс производства белков, которые они должны помогать синтезировать.
Это своеобразное титрование связывающегося белка, происходящее при многих недомоганиях, когда экспрессируется и такой белок, и ген миотонической дистрофии, очень помогает объяснить, почему одно и то же заболевание подобного рода порой по-разному проявляется у разных пациентов. Здесь не идет речь о ситуации из разряда «все или ничего». Какая-то доля связывающегося белка может оставаться свободной для того, чтобы все-таки регулировать свой ген-мишень. И эта доля может оказаться разной — в зависимости от размеров зоны экспансии и от соотношения количества имеющейся в клетке информационной РНК миотонической дистрофии и связывающегося белка16.
Не помешает чуть пристальнее рассмотреть те белки, на которые в конечном счете влияет такая нехватка (на рис. 16.4 это условные белки А, В и С). Пока больше всего подтверждений в этом смысле получили инсулиновый рецептор17, один из сердечных белков18, а также белок скелетных мышц, служащий переносчиком хлорид-ионов через мембраны19. Инсулин требуется для поддержания мышечной массы. Если мышечные клетки не экспрессируют достаточно рецептора, связывающего инсулин, мышцы начинают атрофироваться. Сердечный белок, о котором идет речь, играет важную роль в обеспечении нужных электрических характеристик сердца (об этом известно уже сравнительно давно)20. Перенос хлорид-ионов через мембраны в скелетных мышцах — немаловажная стадия циклов мышечного сокращения и релаксации. Поэтому нарушения в процессах обработки информационных РНК, кодирующих эти белки, вполне согласуются с некоторыми из основных симптомов миотонической дистрофии: увяданием мышц, внезапной летальной остановкой сердца из-за губительных аномалий в сердечном ритме, а также трудностями при расслаблении мышц после их сокращения.
Миотоническая дистрофия — весьма показательный пример того, насколько важна мусорная ДНК для здоровья человека. Хотя мутация происходит в информационной РНК, производимой на основе гена, кодирующего белок, данная мутация практически не влияет на сам этот белок. Мутантная область РНК сама становится патологическим агентом и вызывает заболевание, изменяя характер обработки мусорных областей других информационных РНК.
Скажите «ААААААААА»
При нормальных обстоятельствах нетранслируемые области в конце информационных РНК, кодирующих белки, обладают целым рядом функций. Одна из самых важных связана с процессом, затрагивающим все информационные РНК. «Голые» молекулы информационной РНК могут очень быстро расщепляться в клетке посредством процесса, который возник в нашем организме в ходе эволюции. Его цель — поживее избавлять нас от определенных типов вирусов. Чтобы не расщеплялись нужные молекулы и чтобы обеспечить информационным РНК достаточно долгую жизнь (они должны успеть транслироваться в белок); эти молекулы-посланницы модифицируются почти сразу же после возникновения: к концу информационной РНК добавляется множество следующих подряд нуклеотидных оснований А. Схематически это показано на рис. 16.5. На конце информационной РНК млекопитающих обычно находится около 250 нуклеотидных оснований А. Они нужны для сохранения стабильности молекулы и того, чтобы гарантировать: информационная РНК будет выведена за пределы ядра, где она произведена, и затем будет доставлена в рибосомы, где она транслируется в белок.
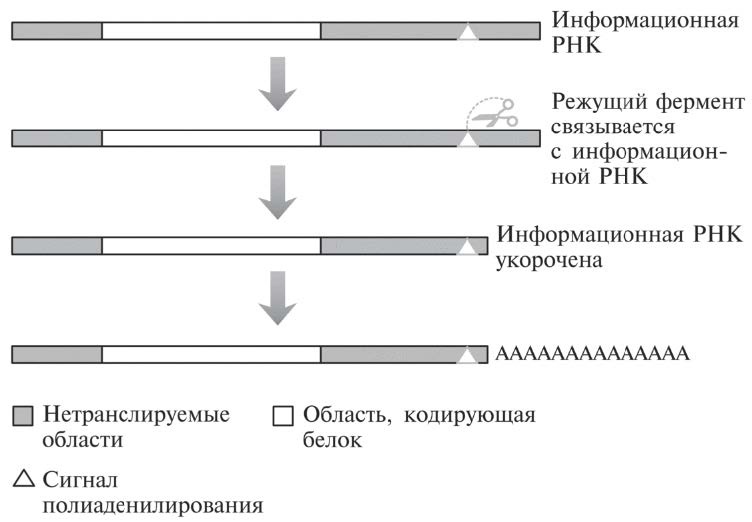
Рис. 16.5. Нуклеотидная последовательность в нетранслируемой области на конце информационной РНК привлекает фермент (обозначен ножницами), который связывается с определенным сайтом и затем отрезает молекулу чуть ближе к ее краю. Множество нуклеотидных оснований А пристраивается к этому укороченному концу молекулы информационной РНК, хотя эти основания не закодированы в исходной ДНК-последовательности.
В конце нетранслируемой области информационной РНК имеется важнейший нуклеотидный мотив (характерная нуклеотидная последовательность). На рис. 16.5 он обозначен треугольничком. Он называется сигналом полиаденилирования (основание А — аденин, поэтому добавление множества оснований А именуется полиаденилированием). Это последовательность из 6 оснований (ААУААА) среди мусора нетранслируемой области. Она служит сигналом для фермента, обрабатывающего информационную РНК (напомним, такая обработка называется процессингом). Распознав этот мотив, состоящий из 6 оснований, фермент отрезает информационную РНК чуть ближе к краю по отношению к тому месту, где располагается мотив (обычно в 10-30 основаниях от него). И затем уже другой фермент может пристроить множество оснований А к оставшейся части информационной РНК
[61].
Тот же мотив из 6 нуклеотидных оснований часто встречается в одной той же нетранслируемой области многократно. Пока не совсем ясно, как клетка «выбирает», каким именно мотивом воспользоваться в том или ином случае. Но раз уж у нее есть выбор из множества мотивов, может иметься и множество информационных РНК, кодирующих один и тот же белок, однако содержащих нетранслируемую область разной длины непосредственно перед этими множественными основаниями А, идущими подряд. Эти информационные РНК разной длины будут обладать разной стабильностью, а значит, вырабатывать разное количество белка. Вероятно, благодаря этому организм получает дополнительную возможность осуществлять тонкую подстройку вырабатываемого количества белка21.
Существует весьма необычная и редкая генетическая болезнь, именуемая IPEX-синдромом
[62]. Это смертельное аутоиммунное заболевание, при котором организм атакует и разрушает собственные ткани. В частности, атаке подвергаются клетки, выстилающие внутреннюю поверхность кишечника, что приводит к острой диарее у младенцев и препятствует их нормальному развитию. Атаке могут подвергаться также железы, вырабатывающие гормоны, что приводит к таким болезням, как диабет первого типа (при котором организм пациента не в состоянии вырабатывать инсулин). Под ударом может оказаться и щитовидная железа, что приводит к снижению общего уровня активности организма22.




