Живые мыши в таких случаях появлялись на свет, если яйцеклетку одновременно снабжали ядром другой яйцеклетки и ядром сперматозоида. Если в яйцеклетку одновременно встраивали два ядра других яйцеклеток или два ядра сперматозоидов, эмбрионы некоторое время развивались, но очень скоро погибали. С генетической точки зрения это выглядело весьма непонятно. Ведь во всех трех системах «восстановленная» яйцеклетка содержала нужное количество ДНК. В смысле ДНК-последовательности нет особой разницы между ДНК сперматозоида и ДНК яйцеклетки. К тому же эксперименты специально проводили так, чтобы донорские яйцеклетка и сперматозоид давали реципиенту по одной X-хромосоме. Во всех трех случаях использовались одни и те же ДНК-последовательности. Однако живое потомство рождалось лишь в том случае, когда эти ДНК-последовательности одновременно предоставляли самец и самка1.
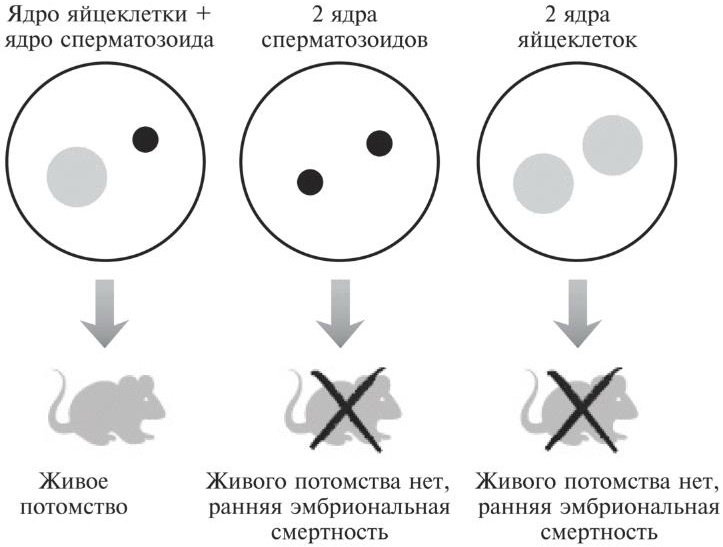
Рис. 10.1. Если в «пустую» яйцеклетку, утратившую собственное ядро, встроить ядро другой яйцеклетки и ядро сперматозоида, в результате появится на свет живая мышь. Если встроить в нее два ядра яйцеклеток или два ядра сперматозоидов, получившиеся эмбрионы не будут развиваться нормально. Однако во всех трех случаях мы имеем дело с одной и той же генетической информацией.
Мы почти уверены, что такое требование одновременного присутствия яйцеклетки и сперматозоида применимо не только к мышам. У человеческих особей встречается заболевание, именуемое пузырным заносом (хориоаденомой, доброкачественной гестационной трофобластической болезнью). Женщина, страдающая им, может казаться беременной, набирать вес, часто испытывать острую утреннюю тошноту. Однако сканирование тела выявляет у нее лишь аномально увеличенную плаценту, полную пузырей с жидкостью, а никакого эмбриона не обнаруживается. В среднем на каждые 1200 беременностей наблюдают один случай пузырного заноса, хотя в некоторых азиатских популяциях этим заболеванием страдает одна из 200 беременных. Возникшее образование спонтанно абортируется примерно через 4-5 месяцев после оплодотворения, хотя в странах с развитой пренатальной медициной врачи удаляют его раньше, чтобы предотвратить развитие потенциально опасных опухолей.
Генетический анализ такой аномалии дает массу ценной информации. Оказывается, в большинстве случаев пузырный занос возникает, когда сперматозоид попадает в яйцеклетку, в которой почему-то нет ядра. Все 23 хромосомы сперматозоида честно копируются, и количество хромосом, как и положено, становится равным 46. Примерно в одной пятой случаев пузырный занос происходит, когда два сперматозоида одновременно проникают в одну из необычных безъядерных яйцеклеток: при этом, опять-таки, в ней оказывается правильное количество хромосом. Как и в вышеизложенных экспериментах с мышами, пузырное образование содержит нужное число хромосом, однако их дает лишь один из родителей, что и приводит к серьезным нарушениям развития эмбриона.
Случаи пузырного заноса и опыты на мышах показали нечто весьма фундаментальное. Они продемонстрировали, что гаметы (яйцеклетка и сперматозоид) снабжают будущий организм еще какой-то информацией помимо генетического кода. Ведь наблюдаемые явления попросту невозможно объяснить, исходя лишь из количества ДНК или характера ДНК-последовательности. В сущности, это явление относится к области эпигенетики. Теперь нам известно, что на молекулярном уровне оно объясняется взаимодействием эпигенетической системы с мусорной ДНК.
Откуда берется ДНК
Ученые обнаружили: некоторые области ДНК несут в себе эпигенетические модификации, как бы сообщающие: «Я — от матери» или «Я — от отца». Это так называемый родительский эффект (parent-of-origin effect). В этих областях генома для нормального развития требуется, чтобы потомок унаследовал одну копию определенного гена (или генов) от матери и одну — от отца.
Такие эпигенетические модификации — не просто голубенькие или розовенькие украшения, показывающие, кто предоставил вам копию гена. Эти модификации контролируют экспрессию определенных генов таким образом, чтобы в каждой паре один включался (скажем, тот, что унаследован от отца), а другой (в данном случае — доставшийся от матери) выключался. Этот процесс называется импринтингом («впечатыванием»): в гены «впечатывается» информация об их происхождении (то есть от кого из родителей они унаследованы).
Обычно то, что клетка экспрессирует две копии гена, кодирующего белок, предоставляет ей своего рода страховку. Даже если одна из копий претерпит мутацию или окажется неправомерно подавленной посредством аномальных эпигенетических модификаций, у клетки все равно останется запасная, нормальная копия. Но если одна из таких копий отключилась из-за импринтинга, клетка становится более подверженной случайному отключению другой копии. Однако некоторые гены в клетке все-таки идут на такой риск, что означает: преимущества импринтинга должны перевешивать его недостатки.
Не случайно такая система возникла лишь у млекопитающих. Самки млекопитающих вносят необычайно большой вклад в развитие своего потомства. Они долго держат детеныша внутри своего тела, делясь с отпрыском питательными веществами через плаценту. Ну да, многие представительницы других классов тоже очень заботятся о своем потомстве. Птицы высиживают яйца, крокодилы хитроумно располагают кладку в гнезде, тщательно регулируя ее температуру. Однако ни у какого другого класса самка не кормит развивающийся эмбрион столь обильно и активно.
Уровень материнской заботливости сдерживается эволюционными причинами. Чтобы успешно передать гены детенышу, самка млекопитающего предпочла бы иметь несколько шансов на такую передачу. Вполне возможно, что ей могут встретиться на жизненном пути другие партнеры, более подходящие (в эволюционном смысле), чем тот, чье потомство она сейчас несет в себе. Поэтому, хотя она многое вкладывает в каждую беременность, самка обладает способностью спариваться неоднократно, что вполне логично. При этом она получит явные эволюционные преимущества, если постарается сделать так, чтобы развивающийся эмбрион (или эмбрионы) получал от нее достаточно питательных веществ. Благодаря этому он будет иметь более высокие шансы на выживание и последующее размножение. Однако не стоит отвлекать на эмбрион такое количество питательных веществ, чтобы их не хватало матери. Во всяком случае, она не должна в результате погибать или утрачивать способность давать потомство.
А вот с самцом история несколько иная. Если его потомок вытянет из матери столько соков, что она больше не сможет размножаться, самцу на это будет, в общем, наплевать. В эволюционном смысле он хочет от наследника лишь одного: чтобы он питался как можно лучше и был как можно сильнее. Тогда у него будут наивысшие шансы на успешное достижение половой зрелости и передачу генов собственным потомкам. Самец, скорее всего, будет спариваться и с другими самками: лишь сравнительно небольшое число видов млекопитающих образует пару на всю жизнь.
Самки млекопитающих не в состоянии решать, какую долю питательных веществ передавать эмбриону, обитающему в утробе. Это вам не птицы — те-то могут раньше времени бросить гнездо. Поэтому эволюция добилась эпигенетического перемирия в этой гонке питательных вооружений. Возник механизм импринтинга, позволяющий сбалансировать конкурирующие требования мужского и женского вклада в геном. У небольшого количества генов эпигенетические модификации ДНК, наследуемой от отца, задают характер генетической экспрессии, способствующий росту эмбриона. Но у тех же генов иной характер генетической экспрессии, задаваемый эпигенетическими модификациями ДНК, наследуемой от матери, оказывает на эмбрион противоположное действие.

