Но какую же кислоту отпустил Вале аптекарь? Вероятнее всего, соляную. Именно соляная кислота продается в аптеке. В 1897 г. российский физиолог Иван Петрович Павлов обнаружил, что желудок человека и млекопитающих вырабатывает соляную кислоту, которая составляет 0,5 % от массы желудочного сока. Людям с пониженной кислотностью желудочного сока прописывали соляную кислоту, которую можно было купить в аптеке. Сейчас 6 %-ная соляная кислота продается в аптеках в составе раствора Демьяновича – средства для лечения некоторых кожных заболеваний. Суть действия этого препарата заключается в реакции, при которой на поверхности кожи выделяется мелкодисперсная сера и сернистый газ, они-то и действуют на причину заболевания, например, на чесоточного клеща. А образуются эти вещества при обработке кожи сначала 60 %-ным раствором тиосульфата натрия, а затем соляной кислотой. При этом происходит реакция:
Na2S2O3 + 2HCl = 2NaCl + S + SO2 + H2O

Соляная кислота – это водный раствор газообразного хлороводорода HCl. Массовая доля хлороводорода в соляной кислоте не может превышать 37 % из-за ограниченной растворимости газов в воде. Соляная кислота называется так потому, что получили ее впервые из поваренной соли прокаливанием ее с железным купоросом FeSO4 ∙ 7H2O:
2(FeSO4 ∙ 7H2O) + 2NaCl = 2HCl + Fe2O3 + Na2SO4 + SO2 + 13Н2О
Этим способом монах-алхимик Василий Валентин в XV в. получил пары, которые при растворении в воде дали то, что мы сейчас называем соляной кислотой, а Василий Валентин назвал spiritus salis (дух соли). Арабским алхимикам этот способ был известен несколькими веками ранее.
Немецкий химик Иоганн Рудольф Глаубер в середине XVII в. заменил в этом рецепте железный купорос на концентрированную серную кислоту и получил значительно более чистую соляную кислоту:
2NaCl + H2SO4 = 2HCl + Na2SO4

В реторте после отгонки соляной кислоты оставалась соль, которую Глаубер растворил в воде и исследовал. Оказалось, раствор соли обладает слабительным действием. Глаубер назвал ее Sal mirabile (удивительная соль). До сих пор ее используют в медицине под названием «глауберова соль». А природный кристаллогидрат Na2SO4 ∙ 10Н2О назвали мирабилитом. По способу Глаубера соляную кислоту получали еще в ХХ в. Надо полагать, именно такую кислоту купил в аптеке Валя Катаев.
Почему нечистый цинк не годится для опыта по получению водорода?
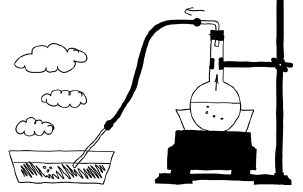
И цинк с примесями, и оцинкованное кровельное железо прекрасно взаимодействуют с кислотой с образованием водорода. Кстати, цинк с примесями свинца и других менее активных металлов с кислотой взаимодействует значительно быстрее, чем химически чистый цинк. Контакт двух металлов разной химической активности в растворе электролита создает так называемую гальваническую пару, в которой более активный металл (в данном случае цинк) окисляется быстрее, а менее активный, наоборот, не окисляется, пока сосед «отвлекает на себя» ионы водорода, выступающие в роли окислителя. Поэтому гранулы цинка, побывавшие в пробирке с кислотой, как бы чернеют: светлый блестящий цинк растворяется, а на поверхности выступают темные кристаллики свинца, висмута и других примесей, не растворяющихся в соляной кислоте. Но почему тогда загрязненный цинк не рекомендуют брать для получения водорода? А потому что примесями к цинку могут быть не только менее активные металлы, но и мышьяк, фосфор, сера. Атомарный водород в момент выделения восстанавливает эти примеси до летучих водородных соединений арсина (AsH3), фосфина (РН3), сероводорода (Н2S). Все эти соединения представляют собой ядовитые газы с неприятными запахами. У чистого арсина нет запаха, но загрязненный имеет чесночный запах. Фосфин обладает «запахом гнилой рыбы», а сероводород имеет «запах тухлых яиц». Он-то, видимо, и выделялся вместе с водородом в опыте гимназиста Катаева, «слегка пованивая чем-то тухлым». Значит, цинк, проданный в аптеке, тоже был загрязнен примесями серы или сульфидов, и опыт был не вполне безопасен. Чтобы очистить водород от примеси ядовитых газов, нужно было бы пропускать его через раствор какого-нибудь окислителя, способного окислить эти газы до безвредных солей. Например, через подкисленный раствор дихромата калия или перманганата калия. А поместить этот раствор следовало бы в двугорлую промывную склянку (склянку Вульфа), соединенную газоотводной трубкой с той склянкой, где бесстрашный экспериментатор получал водород.
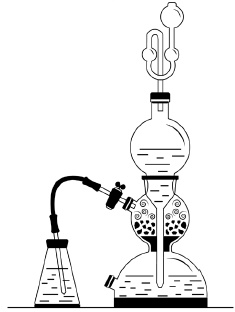
О какой химической посуде идет речь в рассказе?
Восторг, который охватил гимназиста Валентина в магазине лабораторного оборудования, понятен. Стеклянная химическая посуда завораживает совершенством своих форм. Многое из того, чем в начале ХХ в. любовался и даже пользовался незадачливый экспериментатор, изобретено за сотни лет до описываемых событий и до сих пор встречается в химических лабораториях. «Специальный сосуд для соединения цинка с кислотой» – это аппарат Киппа, которым и сейчас пользуются в школьных химических лабораториях. Раньше его форма ассоциировалась у учеников со снеговиком, а сейчас они чаще при взгляде на аппарат Киппа вспоминают кальян. Прибор этот с середины XIX в. производила голландская фирма научных приборов, принадлежавшая аптекарю Петеру-Якобу Киппу, отсюда его название. В аппарате Киппа получают газы действием какого-либо раствора на твердое вещество, если для реакции не требуется нагревание. Прибор устроен таким образом, что при перекрывании газоотводной трубки избыток газа выдавливает кислоту в сферическую воронку и реакция прекращается. Стоит открыть кран, и газ выходит из сферического резервуара, давление в нем падает, кислота возвращается туда, где находится цинк, и снова начинается выделение водорода. То есть реакцию можно в любой момент как остановить, так и возобновить. Это очень удобно и экономно. Но у Валентина не было денег на такой дорогостоящий прибор.